La metformine et la perte de poids

La metformine, médicament de première intention dans le traitement du diabète de type 2, est prescrite à plus de 150 millions de patients dans le monde. Mais ces dernières années, elle est de plus en plus souvent évoquée dans le contexte de la perte de poids. Est-elle efficace comme produit amaigrissant ? La réponse n’est pas claire et nécessite une analyse approfondie.
Une revue systématique et une méta-analyse publiées dans la revue Diabetes, Obesity and Metabolism (Haber R. et al., 2024) ont analysé les données d’études randomisées contrôlées menées chez des patients en surpoidsetobèses sans diabète. Conclusion: la metformine entraîne une perte de poids modeste mais statistiquement significative. Ce n’est pas une révolution. Ce n’est pas une pilule magique. Il s’agit plutôt d’un outil supplémentaire entre les mains d’un médecin compétent.
Échangez avec un médecin agréé en ligne pour un accompagnement personnalisé dans la gestion du poids.
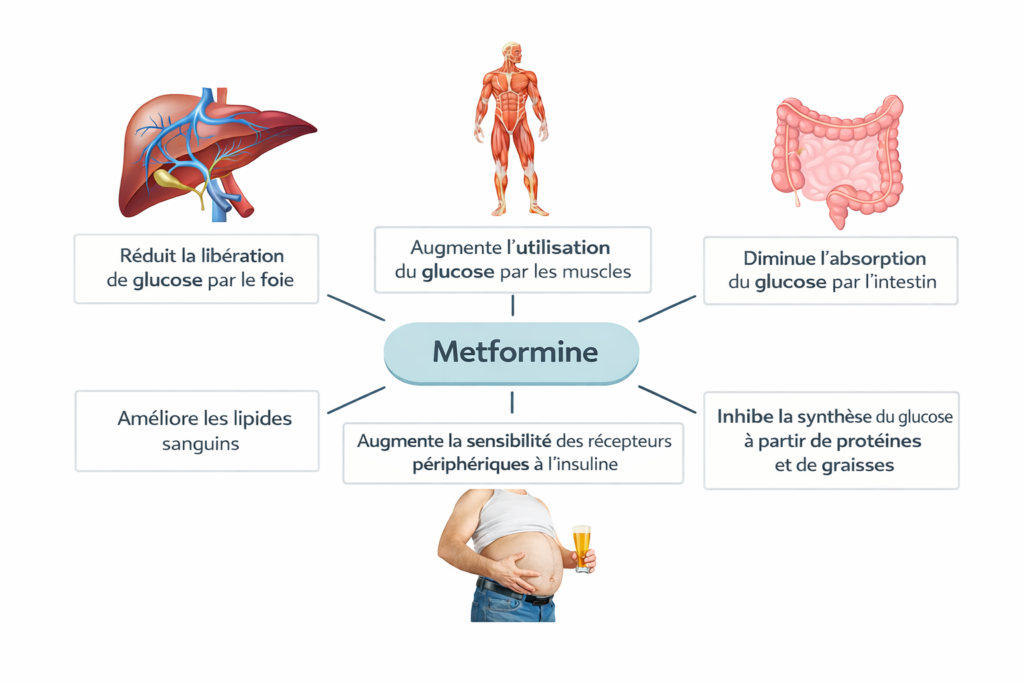
Mécanisme d’action: comment la metformine influence le poids corporel
La metformine réduit la production de glucose dans le foie en inhibant la néoglucogenèse indépendamment de l’insuline. Elle inhibe le complexe I de la chaîne respiratoire mitochondriale, ce qui déclenche une cascade de réactions par l’activation de l’enzyme AMPK. En parallèle, le médicament renforce l’absorption du glucose par les tissus musculaires et ralentit son absorption dans l’intestin.
Mais quel est le rapport avec le poids ? Pendant longtemps, le lien entre la metformine et la perte de poids est resté un mystère. La percée a eu lieu après la découverte de la molécule Lac-Phe – N-lactoyl-phénylalanine.
Qu’est-ce que la molécule Lac-Phe et quel est son rapport avec l’appétit ?
La Lac-Phe est une molécule hybride composée de lactate et de l’acide aminé phénylalanine. Elle a été découverte par des scientifiques de l’université de Stanford lors d’une étude sur les métabolites circulant dans le sang après un effort physique intense. Cette molécule supprime la sensation de faim. L’étude de Xiao S. et al. (2024), publiée dans Nature Metabolism, a démontré que la metformine stimule la synthèse de Lac-Phe dans les cellules de l’épithélium intestinal. La metformine augmente la production du métabolite Lac-Phe dans les cellules intestinales et les muscles squelettiques, et le Lac-Phe intervient, au moins en partie, dans la consommation alimentaire et le poids corporel. Il s’agit en fait d’un mécanisme qui coïncide en partie avec les réactions métaboliques observées après un effort physique très intense.
La metformine réduit-elle réellement l’appétit ou s’agit-il d’un effet secondaire sur le système gastro-intestinal ?
Il n’est pas facile de distinguer ces deux phénomènes. Nausées, malaises abdominaux, diarrhées : autant de symptômes fréquents au cours des premières semaines de traitement. Et oui, ils conduisent naturellement à une diminution de l’appétit. Cependant, les données de l’étude de Stanford indiquent un mécanisme biochimique distinct de suppression de la faim par le Lac-Phe, qui n’est pas lié à des troubles gastro-intestinaux. Chez les souris privées de la capacité de synthétiser le Lac-Phe, la metformine perdait en grande partie son effet sur l’appétit et le poids corporel, tout en conservant toutes ses autres propriétés.
On pensait auparavant que le hormone GDF15, dont le taux augmente sous l’effet de la metformine, jouait un rôle clé dans la régulation de la faim. Mais des expériences sur des souris knock-out ont montré qu’en l’absence de l’enzyme CNDP2, responsable de la synthèse du Lac-Phe, les niveaux de GDF15, GLP-1 et PYY ne différaient pas entre les groupes, et l’effet sur le poids disparaissait. Cela indique que le Lac-Phe joue un rôle central dans l’équilibre énergétique sous metformine.
Chiffres réels: combien de kilos les patients perdent-ils ?
Les patients atteints de diabète de type 2 qui commencent à prendre de la metformine perdent 2 à 3 % de leur poids corporel au cours de la première année. En chiffres absolus, cela représente 3 à 6 kg en monothérapie.
À titre de comparaison:
- Metformine en monothérapie – perte de 2 à 6 % du poids corporel
- Semaglutide (Ozempic, Wegovy) : perte de 15 % et plus
La différence est évidente. La metformine n’est pas en concurrence avec les médicaments injectables de nouvelle génération en termes de perte de poids.
La méta-analyse de Haber et al. (2024) a révélé des données contradictoires chez les patients non diabétiques. L’effet est présent, mais il est moins prévisible et dépend du degré initial d’insulinorésistance. Chez les personnes présentant une insulinorésistance prononcée, la réponse à la metformine peut être plus marquée. Chez les patients sensibles à l’insuline, la perte de poids est souvent minime.
Les données sur la persistance de l’effet après l’arrêt du traitement sont limitées. La plupart des études font état d’une perte de poids au cours des 6 à 12 mois de traitement actif. Après l’arrêt du traitement, le poids revient généralement à la normale si le patient n’a pas modifié ses habitudes alimentaires et son niveau d’activité physique. La metformine ne modifie pas le métabolisme de façon permanente : elle agit tant qu’elle est prise.
La posologie a-t-elle une incidence sur l’ampleur de la perte de poids ?
La dose thérapeutique typique est de 500 à 2000 mg par jour. Les études montrent un effet dose-dépendant : à des doses plus élevées, on observe une augmentation significative du taux de Lac-Phe par rapport aux doses faibles. Mais la fréquence des effets secondaires gastro-intestinaux augmente également avec la dose. Le médecin détermine la dose individuellement, en commençant par la dose minimale et en l’augmentant progressivement.

Effets secondaires et risques liés à une prise prolongée
La metformine est considérée comme l’un des hypoglycémiants oraux les plus sûrs, avec près de 70 ans d’utilisation clinique. Les principaux effets indésirables concernent le système digestif : ballonnements, diarrhée, nausées. Ils touchent jusqu’à 20 % des patients. Ces symptômes apparaissent plus souvent au début du traitement et lors d’une augmentation rapide de la dose.
Un titrage lent et l’utilisation de formes galéniques à libération prolongée (XR) réduisent la gravité des réactions gastro-intestinales.
L’Agence britannique de réglementation des médicaments (MHRA) classe la carence en vitamine B12 comme un effet secondaire fréquent de la metformine, touchant jusqu’à 1 patient sur 10. Le mécanisme est lié à une perturbation de l’absorption du complexe B12-facteur interne dans l’intestin grêle. Les réserves de vitamine B12 dans l’organisme s’épuisent en 2 à 5 ans. La carence entraîne une anémie et une neuropathie périphérique. Il est raisonnable de surveiller le taux de vitamine B12 tous les 2 à 3 ans pour toute personne prenant de la metformine à long terme.
La crainte de la lactoacidose est un héritage de la phenformine, retirée du marché dans les années 1970. Les données actuelles montrent que la fréquence de la lactoacidose sous metformine est extrêmement faible lorsque les contre-indications sont respectées. Une insuffisance rénale sévère, des états aigus avec perturbation de la perfusion tissulaire sont des situations où le risque est réel. Chez les patients dont la fonction rénale est préservée et qui ne souffrent pas de maladies aiguës, la lactoacidose reste un cas isolé.
L’approche de la prescription de la metformine en cas de maladie rénale chronique (MRC) a changé. Auparavant, on l’évitait. Aujourd’hui, elle est prescrite avec prudence en cas de MRC de stade 1 à 3. Une méta-analyse d’études observationnelles montre que chez ces patients, la metformine est associée à une réduction de 29 à 30 % de la mortalité globale et de 20 à 25 % de la mortalité cardiovasculaire. La décision de prescription est prise par le médecin en tenant compte du débit de filtration glomérulaire.
La metformine et l’obésité sans diabète: prescription hors AMM
La metformine est enregistrée comme médicament pour le traitement du diabète sucré de type 2. Sa prescription à des personnes non diabétiques dans le but de perdre du poids constitue une utilisation hors AMM (off-label). Cette pratique existe, mais nécessite une approche réfléchie.
La revue de Petrie et al. (2024) dans Diabetes, Obesity and Metabolism décrit un éventail croissant d’indications : prédiabète, syndrome des ovaires polykystiques (SOPK), diabète gestationnel. Dans tous ces cas, la metformine entraîne une perte de poids modérée en plus de ses principaux effets thérapeutiques, mais l’ampleur de cet effet dépend de la population et du contexte clinique.
La base de preuves la plus importante concerne le SOPK et le prédiabète. Chez les femmes atteintes du SOPK, la metformine réduit l’insulinorésistance, ce qui a un effet indirect sur le poids corporel et le profil hormonal. Dans le cas du prédiabète, une vaste étude intitulée Diabetes Prevention Program a confirmé l’efficacité de la metformine dans la prévention du diabète de type 2 (réduction du risque d’environ 31 %) et la perte de poids qui l’accompagne.
La metformine est un médicament délivré sur ordonnance avec des indications spécifiques. Son utilisation par des personnes en bonne santé sans troubles métaboliques à des fins esthétiques comporte des risques sans bénéfice prouvé. Une perte de poids de 3 à 6 % ne justifie pas un déficit potentiel en vitamine B12, des troubles gastro-intestinaux et la nécessité d’un suivi médical régulier.
En quoi la metformine diffère-t-elle des médicaments modernes utilisés pour traiter l’obésité ?
Le sémaglutide et le tirzepate, des agonistes des récepteurs GLP-1, permettent une perte de poids de 15 à 25 %. La metformine permet une perte de poids de 3 à 5 %. La différence est considérable. Cependant, la metformine a un coût minime et une longue histoire de sécurité. Les agonistes du GLP-1 sont des médicaments injectables coûteux qui présentent leur propre gamme d’effets secondaires. Ce sont des outils différents pour des situations cliniques différentes.
Lien entre la metformine, l’activité physique et le métabolisme
La découverte de la molécule Lac-Phe a révélé un parallèle inattendu : la metformine et l’exercice physique intense utilisent le même mécanisme pour réduire l’appétit. Tous deux stimulent la production de lactate qui, dans les tissus périphériques, en particulier dans l’intestin et les muscles, se combine avec la phénylalanine pour former du Lac-Phe.
Chez les souris sous metformine, le taux de Lac-Phe dans le sang augmentait autant qu’après un effort de sprint et restait élevé pendant plusieurs heures. Cela laisse penser que la combinaison de la metformine et d’un entraînement régulier renforce l’effet sur l’équilibre énergétique. Cependant, il existe encore peu d’études directes sur l’effet combiné chez l’homme.
La metformine reproduit l’un des effets métaboliques de l’effort physique : la stimulation du Lac-Phe. Mais l’activité physique influence des dizaines d’autres paramètres : la masse musculaire, la sensibilité à l’insuline, la densité osseuse, l’état psycho-émotionnel. Ainsi, la metformine n’est pas un « mimétique de l’exercice » neutre et peut influencer de différentes manières l’adaptation à l’effort physique.
Plusieurs études indiquent un effet paradoxal : la metformine affaiblit certaines adaptations à l’effort aérobie, en particulier l’augmentation de la consommation maximale d’oxygène (VO2max). Cela est lié à la suppression du complexe mitochondrial I, le même mécanisme qui assure l’effet hypoglycémiant. La signification clinique de ce phénomène reste sujette à débat.
Le type d’activité physique a-t-il une importance lors de la prise de metformine ?
Les activités intenses et courtes (sprint, entraînement par intervalles) génèrent plus de lactate et stimulent donc la production de Lac-Phe. Les activités aérobiques modérées (marche, course légère) produisent moins de lactate. En théorie, les entraînements très intenses associés à la metformine ont un effet cumulatif sur la suppression de l’appétit. Les données pratiques sur cette question sont encore en cours d’élaboration.
La metformine dans le contexte de la médecine anti-âge
Une ligne de recherche distincte est liée au projet TAME (Targeting Aging with Metformin), un essai clinique qui étudie le potentiel de la metformine comme moyen de ralentir le vieillissement biologique. Ce médicament est considéré non seulement comme un hypoglycémiant, mais aussi comme une molécule aux effets pléiotropiques : anti-inflammatoire, antioxydant et modificateur du métabolisme cellulaire.
La perte de poids n’est qu’un des mécanismes par lesquels la metformine influence les risques associés au vieillissement. L’amélioration de la sensibilité à l’insuline, la réduction de l’inflammation systémique, la modulation de la microflore intestinale sont autant de voies indépendantes. La perte de poids en soi a un effet positif sur les marqueurs cardiométaboliques, mais n’explique pas tout l’éventail des avantages observés de la metformine.
Le projet TAME a été lancé, mais les résultats définitifs n’ont pas encore été publiés. Il s’agit de la première grande étude clinique spécialement conçue pour étudier l’effet de la metformine sur la fréquence des maladies liées à l’âge chez les personnes non diabétiques. La communauté scientifique attend les résultats avec beaucoup d’intérêt. Ceux-ci détermineront si la metformine sera intégrée à la pratique clinique en tant que géroprotecteur ou si elle restera uniquement un médicament antidiabétique.
La metformine réduit-elle le risque de cancer ?
Des études observationnelles démontrent un lien entre la prise de metformine et une diminution de l’incidence de certains types de cancer. Le mécanisme passe par l’activation de l’AMPK et la suppression de la voie de signalisation mTOR, un régulateur clé de la croissance cellulaire. Mais les preuves disponibles se limitent à des données observationnelles. Les études randomisées confirmant l’effet antitumoral de la metformine sont insuffisantes.